La registrazione dei segnali biologici all’interno di una camera iperbarica pone delle sfide tecniche (le pareti di acciaio che la racchiudono attenuano di molto o bloccano completamente i segnali come in una gabbia di Faraday), pratici (lunghi cavi che creano correnti vortice) e la sicurezza (pericolo di scintille da parte della riserva di energia verso l’apparato elettronico all’interno della camera) che possono essere ottenuti attraverso nuove tecnologie senza fili. In questo rapporto tecnico noi presentiamo il disegno e la realizzazione di un sistema Bluetooth per la registrazione elettroencefalografica (EEG) all’interno di una camera iperbarica e descrivono la fattibilità della trasmissione del segnale EEG al di fuori della camera. A differenza dei vecchi sistemi, questa tecnologia permette la registrazione online di segnali amplificati, senza l’interferenza delle correnti vortice. Durante una pratica di questa tecnica, abbiamo misurato l’attività EEG nei diver di professione secondo tre condizioni sperimentali in una camera iperbarica per determinare come l’ossigeno, assunto ad una pressione iperbarica costante di 2.8 ATA, colpisce l’attività bioelettrica. La forza dello spettro EEG stimata dalla veloce trasformazione di Fourier e le fonti corticali dei ritmi EEG stimati dall’analisi elettromagnetica del cervello a bassa risoluzione sono state analizzate in tre diversi valori: respirare acqua a livello del mare; respirare ossigeno ad una profondità simulata di 18 msw, e respirare l’aria a livello del mare dopo la decompressione.
Termini indice: Bluetooth, elettroencefalogramma (EEG), camera iperbarica, tossicità dell’ossigeno, processo del segnale.
INTRODUZIONE
A partire dagli anni Settanta, la registrazione di segnali nelle camere iperbariche presenta numerose sfide pratiche nella valutazione di parametri biologici durante l’addestramento ed in situazioni operative di diver professionali o studenti. La maggiore limitazione sta nel fatto che la camera è chiusa come in un astuccio di acciaio, come una gabbia di Faraday che fa da scudo contro le onde elettromagnetiche entrando dall’ambiente e blocca le onde elettromagnetiche generate dentro dal propagarsi al di fuori. Ciò significa che un generatore di onde elettromagnetiche posizionato dentro alla camera non può essere visto dall’esterno. La seconda limitazione è che la provvigione di equipaggiamento dentro la camera non può essere potenziata dalla corrente alternativa poiché potrebbe generare scintille, creando un consistente problema di sicurezza in presenza di un gas come idrogeno od ossigeno. Quindi, l’equipaggiamento necessita di ricevere potenza attraverso una corrente continua a basso voltaggio e si necessita di prendere speciali precauzioni di sicurezza durante l’apertura e la chiusura del circuito di sopperimento di energia per prevenire la formazione di scintille.
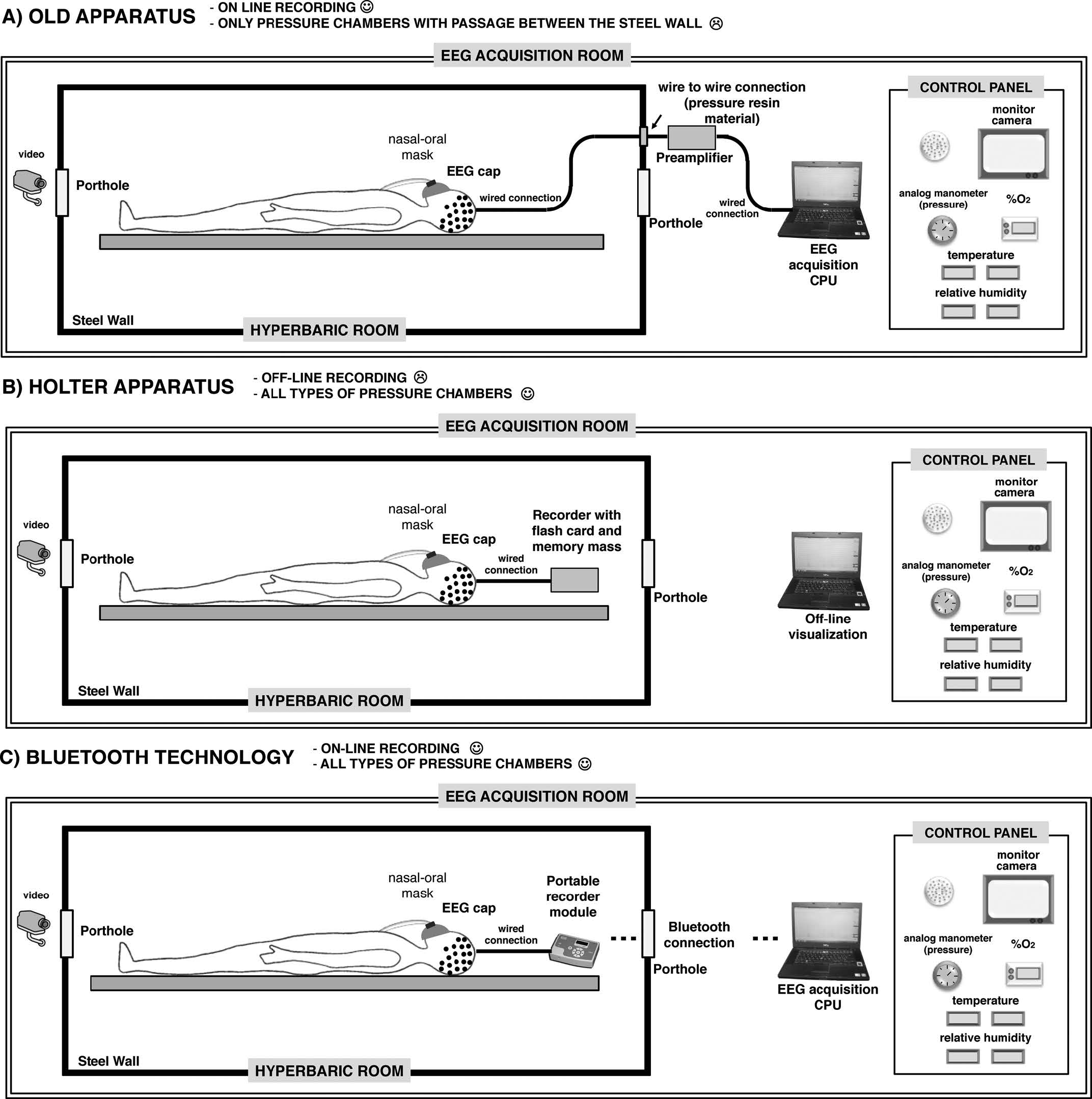
Finora, il problema principale con lo scudo a forma di astuccio di acciaio che fa da scudo alla propagazione di onde elettromagnetiche è stato risolto col far scorrere le connessioni di filo spinato dalle fonti di segnale biologiche, come in un elettrocardiogramma (ECG) od un elettroencefalogramma (EEG), verso il fuori della camera. Una collezione filo a filo (spinato) incluso come in un letto in un materiale in un materiale resistente alla pressione unisce le due cavità, una dentro e l’altra fuori della camera. L’apparato è inchiodato alla parete della camera. Comunque, anche con questa erezione, la registrazione di segnali biologici come EEG (nell’ordine di …) rimane sub ottimale. Passi per migliorare la qualità del segnale EEG implicano il far rimanere la lunghezza del cavo ad un minimo per prevenire interferenze dalle correnti vortice durante la registrazione dell’EEG e nel porre il soggetto umano il più vicino possibile alla parete della camera. Ma poiché i segnali EEG vicini alla fonte di registrazione non possono essere amplificati grazie al pericolo potenziale del verificarsi di scintille dalla riserva di potenza del dispositivo, e poiché unità separate di amplificazione del segnale e della sua registrazione non sono disponibili in commercio, il dispositivo di registrazione ha bisogno di essere collocato tanto vicino quanto in modo pratico nel muro esterno della camera per ridurre le correnti vortice, ed i cavi fuori dalla camera a scudo per ridurre l’interferenza elettromagnetica (Figura 1 a).
Data la miriade di difficoltà nel quantificare il segnale EEG, gli studi EEG sulle camere iperbariche non sono così comuni. L’EEG per la prima volta fu registrato negli animali nel 1945 e negli umani nel 1969, e in modo specifico per lo studio della sindrome nervosa ad alta pressione (HPNS) nel 1968-1969. Nel 1974, Rostain e Naquet misero in pratica studi sull’EEG negli umani per identificare gli effetti del misto di gas all’elio e all’ossigeno; Rostain continuò questa linea di ricerca dal 1974 al 1988, sperimentando l’He/O2 in particolare. Solo di recente l’analisi di Fourier è stata applicata a registrazioni EEG umane in una camera iperbarica per quantificare il segnale EEG.
Con lo sviluppo del monitor dell’Holter, per esempio, un dispositivo di collezione di dati di ambulatorio che amplifichi i segnali (ritmo del cuore) per mezzo di sensori attaccati al petto di colui che li indossa e li registra in una memoria di immagazzinamento rimovibile, si potrebbero risolvere molti di questi svantaggi. Il monitor Holter è rafforzato da una corrente diretta a basso voltaggio (dc) che non genera scintille durante l’apertura e la chiusura del circuito di fornitura della corrente. Inoltre, poiché i segnali si amplificano vicino alla loro fonte, possono essere usati cavi estremamente corti così minimizzando l’interferenza da parte delle correnti vortice; dopo l’amplificazione, i segnali possono essere registrati con migliore accuratezza, ancora, senza l’interferenza delle correnti vortice. Il vecchio “off-line” metodo di registrazione consisteva in una registrazione di memoria di massa che poteva essere letta fuori dalla camera; comunque, il soggetto non poteva essere monitorato in modo “online”, che precludeva un pronto intervento se l’EEG indicava una situazione pericolosa.
Con lo sviluppo del modello di comunicazione Bluetooth, la trasmissione del segnale via onde radio a bassa banda ovviò il bisogno di cavi. Usando lo stesso sistema di comunicazione radio, dispositivi multipli possono comunicare e scambiare dati attraverso connessioni senza cavi per brevi distanze.
Le applicazioni Bluetooth sono ambienti interni, dove l’attenuazione grazie alle pareti e la diminuzione del segnale grazie alla riflessione del segnale possono ambedue ridurre la gamma. Applicata a dispositivi portatili, la tecnologia Bluetooth permette di registrare segnali in linea già amplificati senza l’interferenza delle correnti vortice provocate dai cavi (fig. 1 c)
In questo saggio tecnico, presentiamo un meccanismo Bluetooth che permette la registrazione di segnali biologici in una camera iperbarica nonostante la presenza di una gabbia di Faraday. Sebbene tali sistemi possano essere usati per una gran varietà di propositi, qui ci si concentra sulla loro potenziale applicazione nelle camere iperbariche. Nel dettaglio, un EEG a 32 canali è stato registrato con un sistema EEG Bluetooth in 11 divers di professione. Una registrazione EEG di 20 minuti fu portata a termine secondo tre diverse condizioni sperimentali: l’aria (linea di base a livello del mare, 1 atmosfera di pressione assoluta ATA); assunzione di ossigeno (ad una profondità simulata di 18 msw, 2.8 ATA); ed aria (dopo la decompressione, 1 ATA). Le onde radio a bassa banda Bluetooth riescono ad oltrepassare gli oblò di resina delle pareti della camera iperbarica. I vantaggi della tecnologia senza fili nel trasferire i dati fuori dalla camera iperbarica vengono pure discussi.

Descrizione del dispositivo
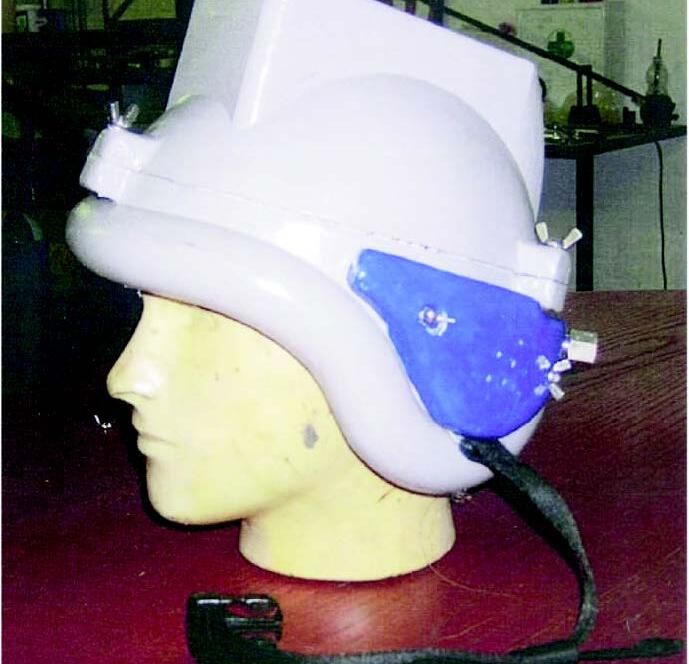
L’equipaggiamento per l’EEG usato in questo studio è un registratore portatile connesso tramite una trasmissione senza fili Bluetooth ad un taccuino che visualizza il segnale EEG (EBNeuro – ATES Medica Device, Verona, Italia) (fig. 2). Il modulo Bluetooth Neurotravel è un modulo di Classe 2 incastonato insieme con una antenna.
Il sistema EEG Bluetooth include un cappelletto o tappo con 32 canali, una unità di acquisizione ed una unità di processo ed immagazzinamento dati. Sebbene lo studio fosse condotto usando il sistema di acquisizione, altri sistemi Bluetooth possono essere probabilmente usati per il medesimo scopo (per esempio: B-Alert X24 EEG SystemEmotiv EPOC, g.Nautilus – sistema senza fili EEG g. tec, Enobio Wireless EEG, eccetera).
L’unità di acquisizione (Neurotravel GEM100/SMART) individua segnali sul soggetto per mezzo di un modulo di acquisizione connesso al taccuino via Bluetooth. Questo moduolo acquisisce campioni dai segnali amplificati provenienti dai canali sul cappelletto. Un filtro anti-aliasing precede la digitalizzazione del segnale EEG a 250 Hz. I segnali vengono registrati con una risoluzione a 16 bit.
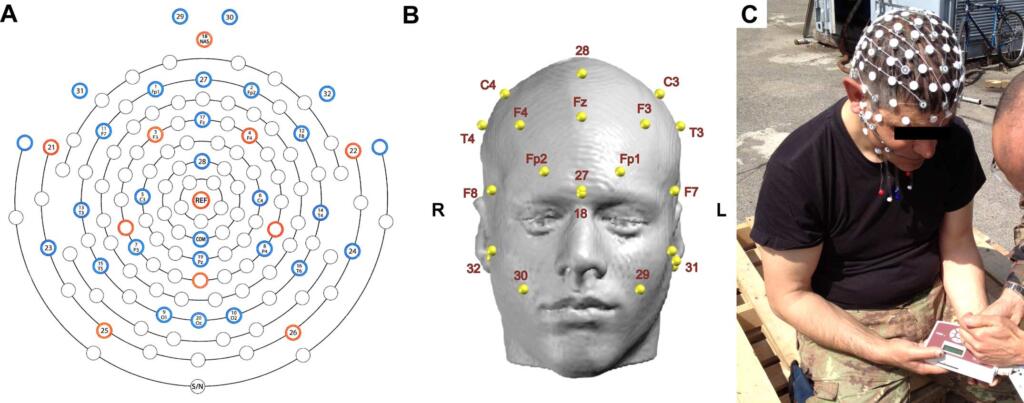
Il cappelletto dell’EEG (Electrical Geodesic Inc., OR, USA) (Fig. 3) è composta da elettrodi Ag/AgCl, che vengono affogati in una soluzione di potassio fisiologico per circa 5 minuti prima dell’inizio della registrazione. La soluzione crea un certo microclima tra lo scalpo del soggetto e gli elettrodi che mantengono basse le impendenze anche durante le lunghe registrazioni dell’EEG. La rete è stata ordinata in modo che 18 (posizionati sul nasione), Cz, Oz, ed i punti preauricolari fossero piazzati correttamente secondo il sistema internazionale 10/20. In virtù della struttura tensiva geodesica della rete, tutti gli elettrodi sono stati distribuiti equamente sullo scalpo. I dati furono registrati contro un riferimento elettrodico di vertice (Cz) ad un campione di 250 Hz usando il software package Geodesic EEG System on Neurotravel Technology (ATES Medica Device, and Electrical Geodesic, Inc.), e in seguito vi si riferì ancora usando la referenza media per l’analisi. Le impendenze degli elettrodi furono verificate e mostrarono insignificanti resistenze nella gamma di 20-80 …
Applicazioni
Tossicità dell’ossigeno
L’uso di un miscuglio di ossigeno e apparato respiratorio a circuito chiuso (CCBA) per immergersi a varie profondità aumenta il rischio di tossicità dell’ossigeno del sistema nervoso centrale (CNS O2T). Il modello EEG è famoso perché cambia in modo significativo durante le immersioni saturative. L’avvelenamento dell’ossigeno si può manifestare con una varietà di sintomi e complicazioni: dalla nausea, stordimento, disturbi dell’udito e della vista, amnesia, vertigini, irritabilità e contorsioni muscolari localizzate fino alla perdita di coscienza, attacchi tonico-clonici, come pure alterazioni dell’EEG incluso un incremento di onde theta, una diminuzione di onde alpha, brevi sonni, ed un certo declino nella performance psicometrica. La prolungata esposizione all’ossigeno iperbarico (HBO) risulterà in paralisi permanente e morte. Per prevenire questa sindrome, il pronto riconoscimento di questi primi sintomi, come descritti dopo una esposizione asciutta o umidificata all’ossigeno, è vitale. Quindi, una delle più importanti applicazioni di una tecnologia EEG Bluetooth in una camera iperbarica è di misurare l’attività EEG e determinare, calcolare come l’ossigeno e le variabili di pressione iperbarica influiscono sull’attività bioelettrica del cervello in sub di professione. Come prima applicazione, abbiamo calcolato come l’ossigeno, inalato ad una pressione iperbarica costante di 2.8 ATA (profondità simulata di 18 msw), influisce sull’attività bioelettrica in sub umani di professione. Questa attività di EEG allora fu paragonata alle condizioni pre e post ossigeno ad 1 ATA di pressione nel respirare aria.
B Soggetti e protocollo sperimentale
L’EEG fu registrato all’interno di una camera iperbarica usando la tecnologia senza fili Bluetooth come descritto sopra (Fig. 1 c). La popolazione in studio era di 11 sub maschi in salute della marina (età media, 46.2 + 4.9 anni). I criteri di esclusione erano una storia medica di problemi respiratori, malattie del sonno, fumatori e sovrappeso. La commissione etica interna dell’università approvò il protocollo sperimentale, ed un consenso orale e scritto fu ottenuto dai soggetti prima di partecipare allo studio.
Una profondità simulata di 18 msw (2.8 ATA) fu scelta per lo studio perché l’esposizione a questa profondità respiratoria è parte di routine dei corsi di training dei sub della marina. La camera iperbarica usata nello studio si confaceva agli standard della marina italiana, per equipaggiamento di sicurezza e procedure di emergenza. Tutti i soggetti vennero studiati individualmente. Essi furono accompagnati durante l’immersione simulata da un tecnico che assisteva il soggetto se necessario e furono monitorati da una televisione a circuito chiuso. Gli stimoli furono sostenuti attraverso l’intera sessione di registrazione somministrando una stimolazione acustica esterna non appena un 30enne mostrava una riduzione di più del 50% del ritmo alfa del background, secondo le regole di calcolo dell’Accademia Americana di medicina del sonno. La procedura fu portata a termine da un esperto neurofisiologo che era pure responsabile nel notare un qualsiasi fenomeno epilettiforme. L’ispezione visiva dei segnali EEG non mostrava anomalie. I sub avevano una saturazione di emoglobina di sangue completa; tuttavia, il vero valore della pressione parziale dell’ossigeno (pO2), che richiede una campionatura arteriale, non può avere luogo all’interno di una camera iperbarica.
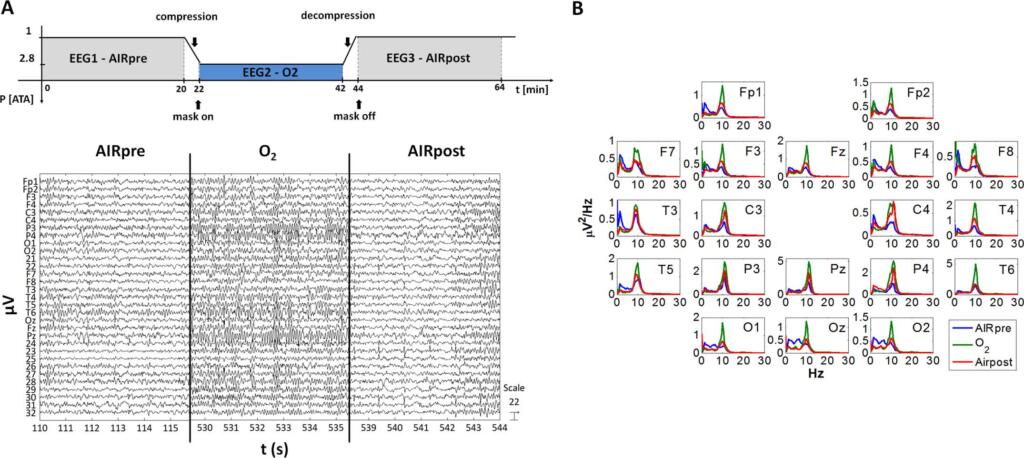
Ciascuna sessione di registrazione durava 20 minuti, durante i quali il soggetto era recline in una cuccetta con gli occhi chiusi. Una registrazione di base dell’EEG fu eseguita ad 1 ATA inalando aria (AIRpre) in una camera aperta. Un profilo di compressione di due minuti (tasso di discesa 9m min -1) respirando aria fu usato per raggiungere la fase dell’ossigeno ad una pressione di 2.8 ATA. A questa pressione, il soggetto respirava ossigeno puro tramite una maschera oronasale (O2) e fu scelta una seconda registrazione di 20 minuti. L’atmosfera all’interno della camera iperbarica fu controllata per mantenere una pressione totale di 2.8 ATA. Dopo la decompressione, di nuovo riguardo la respirazione di aria, l’EEG di ogni soggetto fu registrato per 20 minuti (AIR post), scartando i primi 2 minuti (tasso di ascesa, 9 m min -1). L’intero tempo di tutta la registrazione di EEG fu di circa 1 ora (Fig. 4a). La camera fu compressa di aria ed un circuito respiratorio separato fu usato per la fase dell’ossigeno. Poiché la camera era equipaggiata di un sistema di ventilazione continuo, eventuali falle di ossigeno dalla maschera non si pensava potessero influenzare l’atmosfera all’interno della camera iperbarica (8).
Mappe di scalpo della corrente spettrale dell’EEG
I dati furono riprocessati e processati come descritto in (8). Il potere relativo FFT (%) fu poi stimato per il delta (1-4 Hz), theta (5-7 Hz), alfa (8-12 Hz), beta 1 (13-15 Hz), e beta 2 (15-30 Hz), catene di frequenza.
Il paragone dell’attività del cervello tra il respirare aria al livello del mare (1 ATA) e le condizioni dell’ossigeno (2.8 ATA) negli stessi soggetti mostrava un decremento rapido e significativo nella forza relativa del delta nelle regioni posteriori partendo già dai primi minuti del test, con un incremento parallelo e significativo nel ritmo alfa delle stesse regioni (fig. 4b). Dopo la decompressione (AIR post), il potere relativo del delta scese in modo significativo dal livello base (AIR pre) lungo tutti gli elettrodi fino al minuto 8. Ad 11’-12’, questa diminuzione era localizzata principalmente nelle regioni posteriori. L’incremento nel ritmo alfa era distribuito in modo uniforme sopra alla corteccia cerebrale fino al minuto 8; questo incremento era ancora significativo nelle regioni posteriori fino alla fine dei 20 minuti. Poiché un decremento nell’attività delta durante l’inalazione dell’ossigeno può essere segno di una ridotta performance di meccanismi corticali inibitori, un incremento dell’attività alfa può essere vista nelle regioni centrali dove questa attività è normalmente molto bassa. Durante una esposizione prolungata all’ossigeno iperbarico, i cambiamenti dell’EEG avvennero in tutti i soggetti con una buona riproducibilità. Da ciò si desumerebbe che durante l’inalazione dell’ossigeno la vasocostrizione è seguita dalla vasodilatazione, con un incremento di attività alfa nelle regioni posteriori. Ciò è consono con l’osservazione che la risposta vascolare all’iperossia conduce ad una riduzione del flusso del sangue nel cervello.
D Analisi della fonte corticale dei ritmi EEG.
1)Formazione di immagini Loreta. I dati sono stati preprocessati come prima. I dati EEG per ogni condizione (20 minuti ciascuno) furono divisi in due tempi di 2s. Poiché le bande spettrali di frequenze EEG sono conosciute perché riflettono diverse funzioni e si comportano statisticamente in modo indipendente l’una dall’altra, l’analisi fu condotta separatamente nelle seguenti sei bande: delta (1.5-6 Hz), theta (6-8 Hz), alfa (8-12 Hz), beta1 (12-18 Hz), beta2 (18-21 Hz) e beta3(21-30 Hz). Per localizzare le fonti corticali dell’attività EEG dello scalpo, fu usata una tomografia elettromagnetica del cervello a bassa risoluzione standardizzata (sLORETA http: //www.unizh.ch/keynist 13). Il metodo sLORETA è una soluzione inversa propriamente standardizzata, discreta, distribuita a 3-D, a norma minima. La particolare forma di standardizzazione usata in sLORETA dota la tomografia della proprietà di una esatta localizzazione per testare le fonti principali, sottoponendo le immagini di densità di corrente standardizzata con una esatta localizzazione, sebbene con bassa risoluzione spaziale (per esempio le fonti neuronali saranno altamente correlate).
Nel dominio di frequenza, LORETA può essere computato da spettri trasversali (vedere l’Appendice).
Alle tre condizioni, per ciascun soggetto separatamente e per tutti insieme i soggetti, gli spettri trasversali EEG e poi la corrispondente distribuzione corticale 3-D dei generatori elettrici neuronali furono computati con sLORETA per ogni banda di frequenza. La densità di corrente spettrale fu mappata in una rappresentazione in 3-D: una mappa per ciascuna banda di frequenza nella condizione di AIRpre (1-20 minuti) e sette mappe per l’O2 e le condizioni AIRpost, con 7 intervalli di analisi (1’, 2’, 5’, 8’, 11’, 12’, 16’, 17’, e 19’, 20’). I minuti 19-20 dall’EEG del soggetto n. 3, il minuto 5 dal soggetto n. 8, ed il minuto 2 dal soggetto n. 9, furono scartati grazie ad una perdita del segnale EEG via Bluetooth.
2)Analisi statistica delle soluzioni LORETA. Analisi statistiche furono condotte usando il pacco software sLORETA. La differenza nella localizzazione delle fonti di oscillazioni corticali tra le tre condizioni sperimentali (AIRpre, O2, AIRpost) in ogni banda di frequenza fu stimato da t-test campione indipendenti vossile per vossile su potere di densità di corrente a lungo trasformata sLORETA. Dovuto alla natura non Gaussiana dei dati, nelle risultanti immagini statistiche in 3-D, i vossili corticali che mostrano significanti differenze furono identificate da un approccio non parametrico (mappaggio statistico non parametrico SnPM) via procedimento a casaccio.
Usando questa strategia a casaccio, determinammo i valori soglia di probabilità critica per i valori t veramente osservati con correzione per paragoni multipli tra tutti i vossili e tutte le frequenze. Un totale di 5000 permutazioni furono usate per determinare il significato per ciascun test di randomizzazione. Campioni razionali di media furono usati e considerati con un livello di significato dello 0.95. L’uso di mappe statistiche non parametriche applicato ad immagini LORETA è stato reso valido in studi precedenti. Poiché il metodo LORETA non ha bisogno di alcuna assunzione distributiva, esso attribuisce un valore critico t proprio che ha effetto nel controllare l’errore di tipo 1. Le immagini LORETA furono paragonate statisticamente tra le condizioni (O2 contro AIRpre, AIRpost contro AIRpre). I valori t che corrispondono a p<0.05 furono segnati su uno schema di immagine magnetica a risonanza (MRI) con una barra a scala che indicava potere statistico.
3)Risultati. Una media di soluzioni LORETA (per esempio, densità di corrente relativa presso i vossili corticali) che modelli le fonti distribuite EEG per le bande delta, theta, alfa1, alfa2, beta1, beta2 e beta3 presentava caratteristiche spaziali specifiche durante la respirazione dell’aria in una condizione di stasi e riposo, durante il respiro dell’ossigeno e durante la respirazione dell’aria dopo la fase della decompressione.
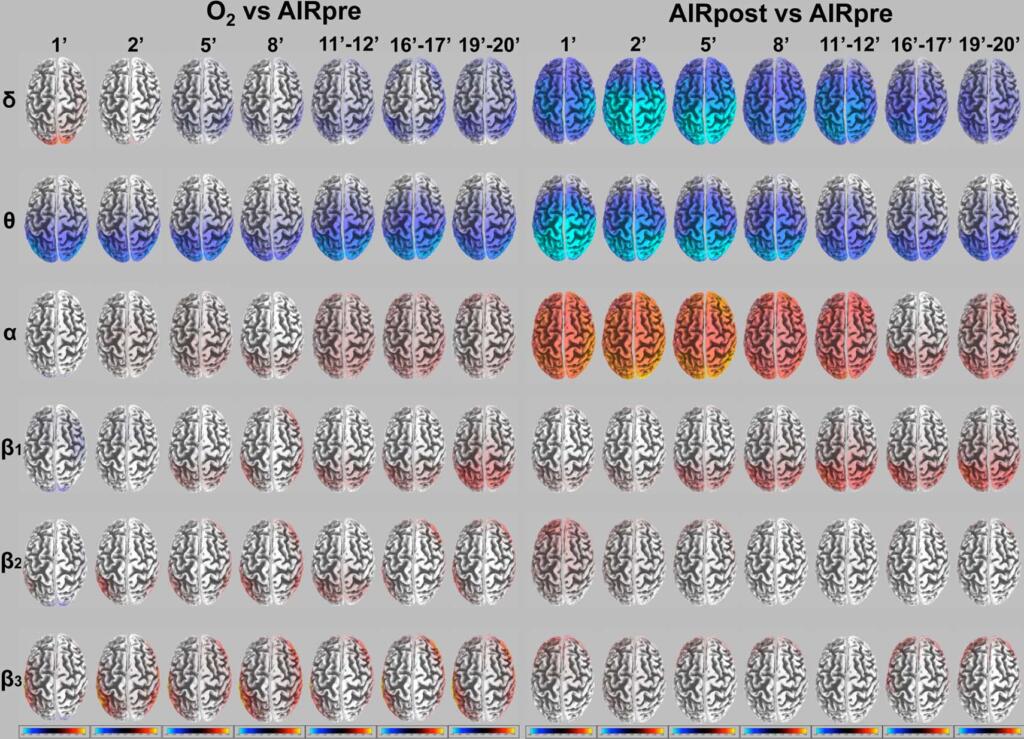
Come paragonato a linea di base, durante l’inalazione dell’ossigeno (2.8 ATA), l’attività del cervello mostrò un decremento rapido e significativo nelle fonti delta e theta nelle regioni posteriori a partire già dai primi minuti dell’inalazione dell’ossigeno ed un incremento parallelo significativo nelle fonti alfa e beta1 nelle stesse regioni (fig. 5). Come mostrato nelle mappe t (O2 contro AIR pre), fu notato un importante decremento per le fonti theta in particolare, e persisteva attraverso l’intera registrazione durante l’assunzione di ossigeno. Soprattutto le fonti alfa, sebbene in modo meno significativo, si localizzavano nelle stesse regioni posteriori. Le bande beta2 e beta3 furono meno coinvolte durante l’assunzione di ossigeno in paragone con la linea di base.
Dopo la decompressione (AIRpost), le fonti delta e theta decrementarono in modo significativo dalla linea di base (AIR pre) principalmente sulle regioni posteriori fino al minuto 5. Ad 11’-12’, il decremento era ancora presente ma meno significativamente sulle regioni posteriori. Dopo 20 minuti, la corrente sembrava quella di AIRpre, anche se non ritornò completamente alla linea di base. Questa modificazione viene mostrata sulle mappe t (AIRpost contro AIRpre). Le fonti alfa e beta1 aumentarono significativamente nelle stesse regioni posteriori durante i primi 2 minuti dopo la decompressione prima di ritornare quasi completamente alla linea di base a 19’-20’. Le bande beta2 e beta3 furono meno coinvolte durante AIRpost come mostra il parallelo con la linea di base.
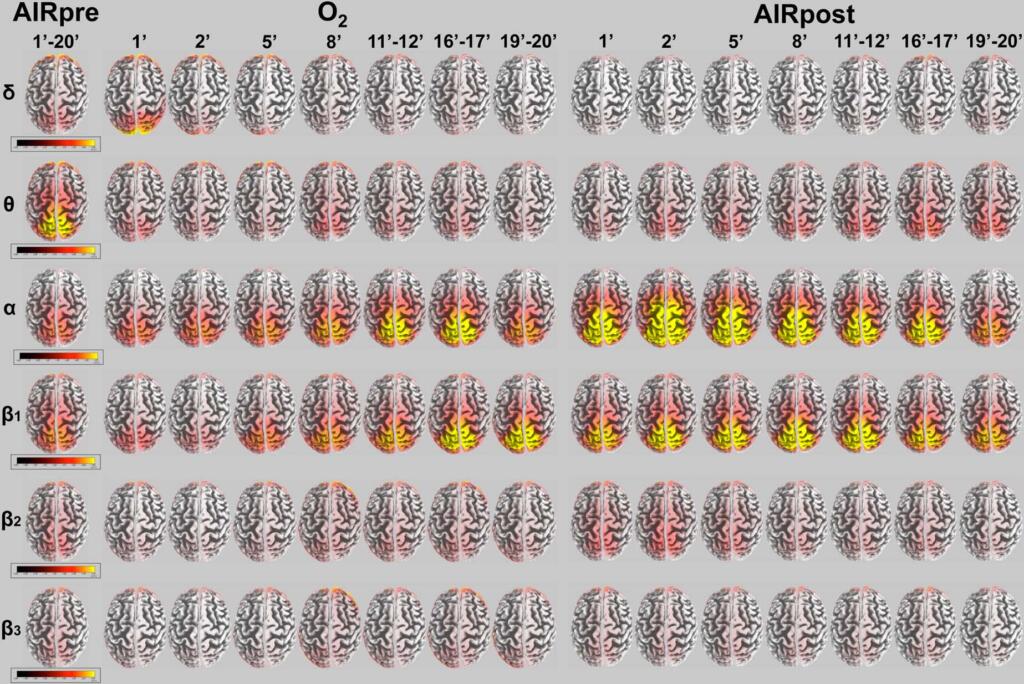
Questi risultati mostrano che l’esposizione ad ossigeno può colpire le fonti corticali dei ritmi dello stato di riposo, per esempio i ritmi lenti decrescono come segno di vasocostrizione segiuti da vasodilatazione, con un incremento nell’attività alfa nelle regioni posteriori. Essi suggeriscono anche che può essere possibile definire e riconoscere segni di attività del cervello tramite induzione di ossigeno, che potrebbe dirigere le decisioni nel trattamento medico di soggetti che mostrino problemi in relazione al diving.
Conclusioni
Sistemi mobili EEG sono stati sviluppati in contesti biomedici per monitorare le condizioni mediche ed hanno anche trovato un posto particolare nelle applicazioni neurologiche (per esempio, epilessia, sonno, interfaccia cervello-computer). Qui ci si concentra sulla loro applicazione potenziale nelle camere iperbariche.
Gli studi sull’EEG nelle camere iperbariche non sono comuni. Le principali limitazioni tecniche sono i problemi pratici con la registrazione del segnale EEG all’interno di una camera racchiusa da acciaio, per esempio una gabbia di Faraday, e che il magazzino di energia dell’equipaggiamento dentro la camera non può essere aumentato dalla corrente alternata a causa del pericolo di scintille.
I vantaggi della tecnologia Bluetooth per la registrazione di parametri geologici in una camera iperbarica sono molti: la qualità del segnale EEG è meglio che nelle vecchie tecnologie perché la trasmissione dei segnali amplificati è meno soggetta ad interferenze ambientali e perché essa permette connessione senza fili senza cavi che possano generare correnti vortice. Le camere iperbariche sono equipaggiate di oblò in Plexiglas resistenti alla pressione attraverso cui le onde radio Bluetooth vengono trasmesse fuori dalla camera. Nel mettere il sistema EEG fuori dalla camera vicino all’oblò, noi possiamo ottenere dati di acquisizione più certi. In aggiunta, i cosiddetti penetratori scafo (consistenti di due cavità connesse filo a filo e incassate nella resina resistente alla pressione), generalmente non sono più forniti sulle camere iperbariche.
I nostri risultati sperimentali indicano che questo sistema dedito può creare una piattaforma EEG con una qualità di acquisizione dei segnali simile ai correnti sistemi EEG. I risultati principali della registrazione dell’EEG nei sub di professione durante tre condizioni diverse (respirare aria dentro una camera iperbarica a livello del mare, respirare ossigeno ad una profondità simulata di 18 msw, e respirare aria a livello del mare dopo la decompressione) hanno mostrato che le fonti corticali sono affette dalla respirazione dell’ossigeno per almeno 20 minuti. La condizione dell’ossigeno era caratterizzata da un marcato incremento di amplitudine nelle fonti alfa e beta1 nelle aree parietali ed occipitali ed un decremento di amplitudine nelle fonti occipitali delta e theta. Questi risultati sono in linea con quelli ottenuti dallo scalpo che mostrava un decremento nella forza relativa dei ritmi lenti ed un incremento nei poteri relativi dei ritmi sostenuti. Queste scoperte supportano l’ipotesi che l’esposizione ad ossigeno a lungo termine può colpire in modo diverso le fonti corticali dell’EEG.
Ci sono molte situazioni in cui il cervello umano è esposto ad iperossia, inclusa la terapia medica, il sub, la salute industriale, e la “salvezza” negli ambienti tossici. La tecnica più diffusa per studiare l’iperossia in una condizione normobarica è la perfusione MRI. Parecchi studi hanno reso noto che il flusso del sangue cerebrale allo stadio sessile (CBF) decresce e la resistenza cerebro-vascolare aumenta durante una acuta esposizione all’iperossia normobarica nei soggetti in salute. Il CBF decresceva indipendentemente dalla pressione arteriale parziale del diossido di carbonio (pCO2), indicando un effetto di iperossia cerebrale e vaso costrittivo indipendente. Sostenendo queste osservazioni, Visser e colleghi monitorarono dal Doppler transcranico, (TDC), la velocità del flusso del sangue nell’arteria centrale destra e scoprirono che la velocità TDC media decresceva durante l’esposizione all’ossigeno iperbarico (HBO) (esposizione di 30 minuti a 2.8 bar di puro ossigeno), probabilmente grazie alla vasocostrizione dei veicoli di resistenza cerebrale, poiché essa aumentava nel soggetto che sperimentava una generale contorsione.
L’EEG è stato usato raramente per la valutazione dell’attività del cervello durante l’iperossia. Visser et al. Descrissero gli effetti dell’esposizione a HBO sull’EEG quantitativo e notarono che i cambiamenti elettrici erano minori e non considerati indicativi di un effetto HBO sul cervello nel gruppo di soggetti sani che non mostravano segni di tossicità. Cambiamenti preconvulsivi dell’EEG furono notati solo in un soggetto che ebbe un contorcimento, ma essi erano così privi di significato e non annunciavano segni clinici. Kaskinoro e colleghi scoprirono che l’ossigeno prolungato somministrato ad alte concentrazioni sotto normale pressione atmosferica e con normale ventilazione non causa un rallentamento significativo dell’EEG o produce una qualsiasi attività epilettiforme nei soggetti in salute dell’EEG.
Diversamente, come osservato dai cambiamenti significativi nell’attività neuronale corticale stabilita dalle nostre registrazioni EEG, noi pensiamo che l’iperossia prolungata in questi soggetti in salute abbia indotto la vasocostrizione seguita da vasodilatazione, con un incremento dell’attività alfa nelle regioni posteriori. Queste scoperte potrebbero sostenere il test di tolleranza dell’ossigeno (OTT) nei sub militari e la valutazione di soggetti con propensione a CNS O2T. In particolare, la procedura OTT della marina italiana espone i sub a 2.8 ATA (la stessa pressione del nostro esperimento) per 15 minuti in una camera asciutta mentre respirano il 100% di ossigeno attraverso una maschera facciale. L’EEG potrebbe essere usato facilmente come biomarcatore per scoprire possibili alterazioni nell’attività elettrica del cervello durante il test, per esempio aumento dell’elettricità aumentato nelle bande a bassa frequenza (per esempio, delta, theta) con riduzioni nelle bande di frequenza più alte (per esempio, alfa, beta) e analisi di fonte di localizzazione anomala (LORETA).
La prima applicazione ha prodotto risultati incoraggianti; comunque, due grandi limiti dello studio meritano una discussione. Primo, noi non possiamo escludere completamente un leggero incremento nei componenti alfa come segno di aumentata sonnolenza durante la durata della registrazione. Nonostante ciò, nei nostri risultati abbiamo osservato un incremento nell’attività alfa, specialmente durante la respirazione dell’ossigeno, ed un quasi completo ritorno alla linea di base alla fine della condizione AIRpost. Da questa modifica transeunte, possiamo affermare che i risultati non erano alterati in modo significativo. Inoltre, l’attività sonnolenza-alfa è tipicamente caratterizzata da decresciuta amplitudine sulle aree occipitali, come si confronta col ritmo veglia-alfa, simultaneo all’apparenza di un modello alfa più lento localizzato sulle regioni anteriori. Diversamente, i nostri risultati hanno dimostrato che l’incremento alfa è localizzato specialmente sulle regioni parietali ed occipitali.
La seconda limitazione è che durante l’esalazione dell’ossigeno i soggetti erano esposti simultaneamente ad alta pressione ed ossigeno puro. Queste due variabili non furono manipolate in modo indipendente e noi non fummo in grado di quantificare gli effetti di ciascuna variabile sui risultati. Quindi, stiamo programmando di includere nel protocollo di studi futuri una valutazione dell’EEG durante iperossia normobarica per determinare come l’ossigeno e la pressione iperbarica, rispettivamente, abbiano a che fare con l’attività bioelettrica in sub umani di professione.